Mujer de 38 años con habla escandida y ataxia
Abril Pulenta - Julieta Marquardt
Sin foto
Valentina Palazzesi - Mariana Lagrutta
Sin foto
Enfermedad actual: Consulta por cuadro de 20 días de evolución, de inicio súbito y curso progresivo caracterizado por inestabilidad en la marcha, requiriendo asistencia para deambular.
Por dicho cuadro, consulta inicialmente en efector de su localidad, donde cursó internación por 72 horas con tomografía de cráneo y columna cervical sin alteraciones de jerarquía, otorgándole el alta hospitalaria.
De 10 días de evolución aproximadamente, agrega alteración en el habla (habla escandida) y exacerbación de su cuadro clínico, por lo que es derivada a nuestro efector.
Niega cefalea, fiebre, hipoacusia, disminución de la agudeza visual, diplopía, diarrea, tos, disnea y otros síntomas.
Antecedentes personales:
- Enfermedades del adulto:
- Hipotiroidismo diagnosticado en 2023.
- No adherente a controles de salud.
- Internaciones previas: solo en contexto de cesáreas.
- Antecedentes gineco-obstétricos:
- Gestas 3, cesáreas 2, abortos 1.
- Sin uso de métodos anticonceptivos. FUM: durante la consulta.
- Antecedentes Traumáticos: Niega.
- Antecedentes Quirúrgicos: Niega.
- Antecedentes Alérgicos: Niega alergia medicamentosa
- Medicación habitual: Levotiroxina 50 mcg/día (inicio hace 1 mes aproximadamente
- Vacunación: Sars Cov 2, única dosis.
- Hábitos tóxicos: tabaquista 7 paq/año. Consumidora de alcohol ocasional. Niega consumo de otras drogas
Antecedentes familiares:
Padre: Desconoce
Madre: Desconoce
Hermanas/os: No posee
Hijos/as: Sanos
Examen físico:
- Impresión general: Buen estado general.
- Signos vitales: TA 110/60 mmHg, FC 107 lpm, FR 16 rpm, T° 36.7 ºC, SatO2 98% (0.21)
| Peso: 80 kg | Altura: 1.55 cm | IMC: 33.3 |
- Piel: Máculas hiperpigmentadas faciales, sin cicatrices.
- Cabeza: Ojos: conjuntivas rosadas, escleras blancas. Movimientos oculares no dolorosos. Fosas nasales: permeables sin secreciones ni epistaxis. Puntos sinusales negativos. Cavidad bucal: mucosas húmedas. Lengua central sin lesiones. Piezas dentarias en mal estado.
- Cuello: cilíndrico, simétrico, no se palpan adenopatías ni tiroides. Sin ingurgitación yugular. Pulsos carotídeos simétricos, sin soplos. Acantosis nigricans.
- Tronco: diámetro anteroposterior normal, sin cicatrices. Mamas: sin nódulos ni depresiones, ni secreción por pezón. Columna: sonora, indolora. Puño-percusión: negativa bilateral.
- Aparato Respiratorio: respiración costo abdominal, sin utilización de músculos accesorios, reclutamiento abdominal, tiraje intercostal/supraclavicular, ni aleteo nasal. Expansión de bases y vértices conservada. Excursión de bases conservadas. Sonoridad conservada. Murmullo vesicular conservado, sin ruidos agregados.
- Aparato Cardiovascular: ritmo cardíaco regular, ruidos cardíacos normofonéticos, sin soplos ni R3/R4.
- Abdomen: abdomen globuloso a expensas de panículo adiposo, sin estigmas de circulación colateral ni cicatrices. Blando, depresible e indoloro. Sin visceromegalias. Timpanismo conservado. Traube libre Ruidos hidroaéreos conservados.
- Neurológico: Vigil, orientado en tiempo, espacio y persona. Lenguaje: nómina y repite, palabra escandida. Comprende: comandos y órdenes complejas. Pupilas: isocóricas reactivas y simétricas. Nistagmo horizonto-rotatorio, excepto en la supra abducción. Movimientos oculares externos: completos. Pares craneales: impresionan conservados. Reflejos osteotendinosos: Hiperreflexia rotuliana bilateral. Sensibilidad: táctil superficial conservada. Coordinación: Dismetría a la prueba dedo nariz. Hipermetría en la prueba tobillo rodilla. Respuesta plantar: indiferente bilateral. Hoffman: positivo bilateral. Marcha: aumento de la base de sustentación, inestable. Romberg ps. Sin signos meníngeos.
- Extremidades: Superiores: Tono, trofismo y movilidad conservados. Pulsos conservados. Sin edema ni adenopatías. Inferiores: Tono, trofismo y movilidad conservados. Homans y Ollows negativos. Sin edemas ni adenopatías.
- Región Perineal y genital: vulva e introito sin lesiones ni secreciones.
Exámenes Complementarios previos:
- Tomografía cráneo y columna sin contraste (internación previa): CRÁNEO: No se observan sangrados axiales ni extra axiales. Línea media respetada. Las cavidades ventriculares son de tamaño y morfología normal. La relación sustancia blanca/gris no está alterada. Los surcos corticales son visibles. A nivel de la fosa posterior, el cuarto ventrículo está en línea media y tiene tamaño normal. Cavidades aéreas del cráneo libres. Sin lesiones óseas evidentes. COLUMNA CERVICAL : Relación occipitoatloideo y atloaxoidea conservada. Conducto endomedular respetado. Espesor de tejidos blandos prevertebrales conservados. Sin lesiones óseas evidentes.
Exámenes Complementarios:
| Laboratorio: | Dia 0 | Día 6 | Día 8 |
| Hemoglobina (g/dL) | 13.8 | 14.3 | 13.1 |
| Hematocrito (%) | 41 | 41 | 37 |
| VCM (fl) | 79.3 | 79.3 | 79 |
| HCM (pg) | 26.7 | 27.4 | 27.8 |
| Glóbulos blancos (/mm) | 6340 | 14870 | 12560 |
| Neutrófilos (%) | - | 92 | 87 |
| Eosinófilos (%) | - | 0 | 0 |
| Basófilos (%) | - | 0 | 0 |
| Linfocitos (%) | - | 5 | 7 |
| Monocitos (%) | - | 2 | 4 |
| Plaquetas (/mm) | 315000 | 376000 | 360000 |
| Glicemia (mg/dl) | 76 | 209 | 94 |
| Urea (mg/dl) | 19 | 27 | 32 |
| Creatinina (mg/dl) | 0.68 | 0.68 | 0.64 |
| Sodio (mEq/l) | 137 | 136 | 138 |
| Potasio (mEq/I) | 3.69 | 3.53 | 3.90 |
| Cloro (mEq/l) | 99 | 99 | 100 |
| Calcio (mg/dL) | 9.6 | - | |
| Fósforo (mg/dL) | 3.3 | - | |
| Magnesio (mg/dL) | 1.8 | - | |
| Bilirrubina total (mg/dL) | 0.65 | - | 0.31 |
| TGO (UI/L) | 32 | - | 21 |
| TGP (UI/L) | 84 | - | 90 |
| FAL (UI/L) | 68 | - | 57 |
| GGT (UI/L) | 24 | - | 26 |
| Amilasemia (UI/L) | - | - | 24 |
| VES (mm/1° hora) | 9 | - | - |
| PCR (mg/L) | 0.6 | - | - |
| TP (seg) | 13.6 | 13 | 14.2 |
| KPTT (seg) | 27 | 25 | 25 |
- Radiografía tórax frente (Dia 0): centrada, bien inspirada y penetrada. Indice cardiotorácico conservado.No se observan infiltrados pleuroparenquimatosos. Senos costofrénicos y cardiofrénicos libres.
- Serología VIH (Día 0): No reactivo
- Serología VHB (Dia 0): No reactivo
- Serología VHC (Dia 0): No reactivo
- VDRL suero (Dia 0): No reactivo
- Tirotrofina (TSH) (Dia 0): 1.42 uUI/ml (VN: 0.27-4.20)
- T4 libre sérica (T4L) (Dia 0): 1.49 ng/dl (VN: 0.93-1.7)
- Dosaje de ácido fólico (Dia 0): 18 ng/ml (5.39-20)
- Dosaje de vitamina B12 (Dia 0): No se disponen reactivo.
- Angio RMI de cráneo (Dia 2): Se visualizan lesiones en la sustancia blanca subcortical de centros semiovales y coronas radiadas, hiperintensas en T2/FLAIR, sin restricción en difusión/ADC, de aspecto inespecífico. Podrían estar en relación a trastorno de la microvasculatura, de larga data. Las regiones ganglio basales son de características habituales. El sistema ventricular supratentorial es de forma tamaño y situación normal.En la fosa posterior el 4º ventrículo es de forma tamaño y situación normal. No se observan alteraciones en la intensidad de la señal hemisferios cerebelosos los cuales son de morfología habitual. El tronco encefálico no mostró alteraciones. En la secuencia angiográfica 3D TOF se observa dilatación sacular en la porción inferior del segmento supraclinoideo de la arteria carótida interna izquierda, que mide 2.2 mm, con un cuello de 2.6 mm. Agenesia arteria comunicante posterior izquierda. Las restantes estructuras vasculares del polígono de Willis, son de trayecto calibre y señal flujo conservados, no identificándose alteraciones.
- Cito fisicoquímico de líquido cefalorraquídeo (Dia 2): color y aspecto límpido incoloro. Glucorraquia: 0.56 g/l. Proteinorraquia: 0.28 g/l. Pandy negativo . Elementos: 12/mm3. Tinta china: no se observan elementos levaduriformes compatibles con Cryptococcus sp. . VDRL: no reactiva.
- PCR Virus varicela zoster, Virus Herpes simplex tipo I y II en LCR (Dia 2): No reactivos
- Fracción C3 complemento (Dia 2): 121 mg/dl (VN: 103-145)
- Fracción C4 complemento (Dia 2): 17 mg/dl (VN: 20-50)
- Factor antinuclear (FAN) (Dia 2): No reactivo
- Mycoplasma pneumoniae anticuerpos IgG y IgM (Dia 2): No reactivo
- Gonadotrofina coriónica humana (Dia 5): < 1 mUI/ml
- Anticuerpos anti Gliadina (AGA IgA) (Dia 5): pendiente
- Acs anti transglutaminasa tisular IgA (atTG) (Dia 5): pendiente
- Ecografía ginecológica (Día 9): Útero en antero- verso-flexión, de tamaño conservado. Miometrio heterogéneo, se visualiza en cara anterior fúndica una imagen hipoecogénica, redondeada, intramural, que mide 13.6 mm, compatible con núcleo miomatoso. Endometrio lineal. Ambos ovarios de características ecográficas conservadas. Fondo de saco de Douglas libre.
Evolución:
Curso internación en sala general y fue evaluada en conjunto con servicio de Neurología por síndrome atáxico en estudio. A su ingreso, se realizó Angio resonancia de cráneo que no evidenció alteraciones, se realizó una punción lumbar sin hallazgos de jerarquía, con posterior resultado negativo para virus de varicela zoster y herpes simple.
Al día 5 de internación se realizó pulso de metilprednisolona por 3 días, sin evidencia de mejoría posterior.
Por mantenerse estable clínicamente se decide su alta hospitalaria, debiendo seguir control estricto por consultorio externo con ambos servicios tratantes
Pendientes:
- Resultado anticuerpos pendientes.
- Seguimiento en consultorio externo por equipo de Neurología y clínica Médica
Cuando hablamos de síndrome cerebeloso nos referimos a la disfunción del cerebelo y sus conexiones. Dicho esto, ¿Qué función cumple el cerebelo?. Inicialmente, se creía que las funciones radican en el control de la sensibilidad y la motricidad. Sin embargo, hoy el “síndrome cerebeloso” no es solo motor, sino que integra estos tres grandes ejes: sensoriomotor – cognitivo – afectivo.
Es importante pensar en la afectación topográficamente: el cerebelo se divide en dos hemisferios y el vermis, que se ocupan de funciones diferentes: los hemisferios controlan el tono postural y marcha, mientras que el vermis está implicado en el lenguaje, la coordinación final, los movimientos rítmicos. Por lo tanto, podemos afirmar que la afectación de la paciente corresponde a una pancerebelitis.
Para la evaluación de los síndromes cerebelosos, existen una serie de escalas: las más relevantes son incluyen la international cooperative ataxia rating scale (ICARS) la que evalúa: oculomotor, discurso, movilidad y postura, permitiendo la clasificación en leve moderada y grave. Como punto en contra, requiere una evaluación precisa. Por otro lado, Scale for the assessment and rating ataxia (SARA) evalúa los mismos parámetros, sin tener en cuenta lo oculomotor. Todo esto nos permite la evaluación específica y permitiendo un enfoque más objetivo.
Existe una amplia gama de causas del síndrome cerebeloso. En primera instancia, debemos clasificarlo según el tiempo de evolución: agudo, subagudo y crónico.
Vamos a enfocarnos en la causa subaguda que nos interpela con esta paciente.
Dentro de la variedad de causas subagudas, se pueden clasificar según su etiología en adquiridas, hereditarias, degenerativas.
En las patologías adquiridas podemos nombrar a las causas estructurales y vasculares (descartadas por presentar resonancia sin alteraciones), infecciosas (no presenta signos clínicos ni de laboratorio que nos hagan sospecharla), carenciales ( más frecuentes en pacientes con alteraciones del tracto digestivo), metabólicas (nuestra paciente presenta una analitica sin alteraciones que lo justifiquen), trastornos autoinmunes sistémicos (alejado por no presentar otra sintomatología), tóxicas e inmunomediadas.
Me voy a referir solo a las causas que no fueron descartadas previamente en nuestra paciente.
Nombrando brevemente las causas tóxicas, la intoxicaciones por tolueno (componente de los pegamentos) puede ser causante, sin embargo, lo descarto ya que específicamente la composición del pegamento que la paciente utilizaba para su trabajo, por lo tanto lo descarto.
Existe un reporte de un caso, en 1989 en Eur Neurology, “ataxia as the only delayed neurotoxic manifestation of organophosphate insecticide poisoning” en el que un paciente como manifestación de una intoxicación crónica por organofosforado presenta solo ataxia, sin síndrome colinérgico. De igual forma, el inicio súbito de la sintomatología y la rareza del mismo nos permite alejar esta como causa.
Es interesante enfocarse en las causas inmunomediadas. Las mismas incluyen un grupo de enfermedades que pueden tener atrofia en las imágenes, no pudiendo visualizarse en los estadios más tempranos y con citofisicoquimico de líquido cefalorraquídeo que puede tener pleocitosis leve y bandas oligoclonales.
Considero importante nombrar tanto las que tienen disparadores claros como las que no lo tienen definidos.
Disparadores claros:
- Ataxia por gluten: El diagnóstico se realiza con anticuerpos antigliadina negativos, se descarta el mismo.
- Encefalopatía de Hashimoto: descartada por anticuerpos antitiroideos negativos.
- Cerebelitis postinfecciosa: queda alejada ya que no hay evidencia y tras múltiples interrogatorios, la paciente niega sintomatología viral.
- Degeneración cerebelosa paraneoplásica: Las ataxias paraneoplásicas merecen mención especial: se dan principalmente en mujeres, generalmente se relacionan a cáncer de células pequeñas pulmonar, de mama, ovario o linfoma de hodgkin, existen diferentes autoanticuerpos onconeuronales (anti-Yo, anti-Hu, anti-Tr, anti-Ri, entre otros cuya positividad nos indican diferentes tipos de neoplasias. Hasta un 70% de las veces, se presenta previo al tumor. Típicamente se presentan de forma subaguda, progresiva y no remitente, llevando a grave discapacidad en pocos meses; con frecuencia se detectan) y la respuesta al tratamiento inmunosupresor o al control del tumor es pobre. Su diagnóstico definitivo es la demostración de los anticuerpos onconeuronales, pero hasta en el 40% de los casos son negativos.
Un estudio publicado European journal of neurology (9) plantea que la negatividad de los anticuerpos no excluye el diagnóstico y que la diferencia tanto clínica como de pronóstico no plantea diferencias sustanciales entre las seronegativas y seropositivas.
Generalmente son enfermedades progresivas cuyo tratamiento radica en la inmunomodulación y el tratamiento oncológico y/o quirúrgico. El pronóstico de estas enfermedades suele ser malo. Esto nos plantea la necesidad de realizar screening oncológico en este tipo de pacientes.
Sin disparadores definidos:
- Ataxia asociada a anticuerpos contra la descarboxilasa del ácido glutámico (GAD): La ataxia asociada a anticuerpos anti-GAD es una forma esporádica y poco frecuente de ataxia cerebelosa que se ha descrito en pacientes con inicio entre los 20 y los 70 años. El inicio puede ser subagudo, pero se han notificado casos de ataxia que progresa lentamente a lo largo de los años. Por el curso de evolucion y la edad de la paciente, alejamos el diagnóstico.
- Ataxia cerebelosa primaria autoinmune (PACA): se trata de una ataxia inmunomediada que no tiene desencadenante ni anticuerpos patógenos (Agregado por el Dr. Botasso, aun descritos). Predomina la afectación en vermis. Dentro de los criterios para el diagnóstico se incluyen: pleocitosis, trastornos inmunológicos personales o en familiares de primer grado, autoanticuerpos (sin evidencia de participación en ataxia), exclusión de otras causas alternativas.
Cuando hablamos de la ataxia cerebelosa inmunomediada, puede tener diferentes cursos clínicos (6):
- Recuperación total
- Recuperación parcial
- Estable
- Intermitente
- Gradualmente progresivo
- Rápidamente progresivo
Es relevante también decir que podemos hablar de la “reserva cerebelosa” como la capacidad para restaurar la función perdida. Está es inversamente
proporcional al tiempo de inicio de la sintomatología. Por ende, la inmunoterapia tiene como objetivo detener la progresión y hacerlo de forma temprana permite la remisión completa de la sintomatología.
Cabe destacar que la inmunomodulación puede no tener mejoría clara, sino que se recomienda la combinación de inmunomoduladores. La primera línea de tratamiento es corticoterapia, inmunoglobulina y en casos de convulsiones o status, plasmaféresis (aunque no existe evidencia de clara mejoría con la utilización de la última). De segunda línea, cuando no existe mejoría en las formas rápidamente progresivas a los 10 días, se plantea la realización de rituximab, ciclofosfamida o ambas de ser necesario.
La guía de utilización de inmunoglobulinas en neurología (4) plantea inicialmente y a destacar, que la eficacia de los resultados debe ser medible objetivamente (por ejemplo con las escalas clínicas planteadas anteriormente. En caso de no poder objetivar mejoría, el tratamiento debe ser detenido.
Dicho esto, plantea que en la ataxia degenerativo paraneoplásica, no se realiza tratamiento agudo de rescate con inmunoglobulinas pero si para mantenimiento y deben realizarse concomitantemente con quimioterapia. En la ataxia cerebelosa primaria autoinmune, se realiza el tratamiento agudo y pueden repetirse los cursos de inmunoglobulina.
Las ataxias cerebelosas hereditarias incluyen un grupo heterogéneo de enfermedades genéticas, tanto autosómicas recesivas como dominantes. Recordemos que nuestra paciente desconoce a sus padres biológicos, por ende, no quisiera sacar conclusiones apuradas. Sin embargo, en general los casos de ataxia hereditaria tienen un curso crónico. Además, en las guías de las mismas plantean que es el último diagnóstico a considerar, habiendo descartado otras causas previamente. Es por esto que parece de mayor jerarquía la búsqueda de otra causa antes de considerar realizar el panel genético.
Como conclusión, me parece fundamental contextualizar el conocimiento en la paciente, priorizando los estudios que permitan descartar diferentes causas. La pregunta más importante no es ¿qué tiene?, es, en cambio, ¿cómo seguimos? Recordando que la evolución clínica nos marca el tiempo.
- Bodranghien, F., Bastian, A., Casali, C., Hallett, M., Louis, E. D., Manto, M., Mariën, P., Nowak, D. A., Schmahmann, J. D., Serrao, M., Steiner, K. M., Strupp, M., Tilikete, C., & Timmann, D. (2016). Consensus paper: Revisiting the symptoms and signs of cerebellar syndrome. The Cerebellum, 15(3), 369–391. https://doi.org/10.1007/s12311-015-0687-3
- Abele, M., Bürk, K., Schöls, L., Schwartz, S., Hartmann, T., Besenthal, I., Dichgans, J., Zühlke, C., Riess, O., & Klockgether, T. (2002). The aetiology of sporadic adult-onset ataxia. Brain, 125(5), 961–968. https://doi.org/10.1093/brain/awf107
- Zuberbühler, P. (2010). Ataxia esporádica de comienzo en el adulto: Clasificación y criterios diagnósticos. Neurología Argentina, 2(2), 136. https://doi.org/10.1016/S1853-0028(10)70042-2 ScienceDirect+1
- Mitoma, H., Hadjivassiliou, M., & Honnorat, J. (2015). Guidelines for treatment of immune-mediated cerebellar ataxias. Cerebellum & Ataxias, 2, 14. https://doi.org/10.1186/s40673-015-0034-y BioMed Central
- Mitoma, H., Manto, M., & Hampe, C. S. (2019). Immune-mediated cerebellar ataxias: Practical guidelines and therapeutic challenges. Current Neuropharmacology, 17(1), 33–58. https://doi.org/10.2174/1570159X16666180917105033 benthamdirect.com
- Mitoma, H., Manto, M., & Hampe, C. S. (2017). Immune-mediated cerebellar ataxias: From bench to bedside. Cerebellum & Ataxias, 4, 16. https://doi.org/10.1186/s40673-017-0073-7 PMC+1
- Mitoma, H., Hadjivassiliou, M., Honnorat, J., Graus, F., Sabater, L., Dalmau, J., … Manto, M. (2020). Diagnostic criteria for primary autoimmune cerebellar ataxia (PACA): Guidelines from an International Task Force on immune-mediated cerebellar ataxias. The Cerebellum. Advance online publication. DOI
- Tohid, H. (2016). Anti-glutamic acid decarboxylase antibody positive neurological syndromes. Neurosciences, 21(4), 297–304.
- Ducray, F., Demarquay, G., Graus, F., Decullier, E., Antoine, J.-C., Giometto, B., Psimaras, D., Delattre, J.-Y., Carpentier, A. F., & Honnorat, J. (2014). Seronegative paraneoplastic cerebellar degeneration: The PNS Euronetwork experience. European Journal of Neurology, 21(5), 731–735. https://doi.org/10.1111/ene.12368 PubMed+1
- Graus, F., Vogrig, A., Muñiz-Castrillo, S., Antoine, J.-C., Desestret, V., Dubey, D., … Honnorat, J. (2021). Updated diagnostic criteria for paraneoplastic neurologic syndromes. Neurology: Neuroimmunology & Neuroinflammation, 8(4), e1014. https://doi.org/10.1212/NXI.0000000000001014 Neurology
- Binks, S., Klein, C. J., & Pittock, S. J. (2022). Paraneoplastic neurological syndromes: Clinical presentations and management. Practical Neurology, 22(1), 19–30. pn.bmj.com
No hay información de la evolución.
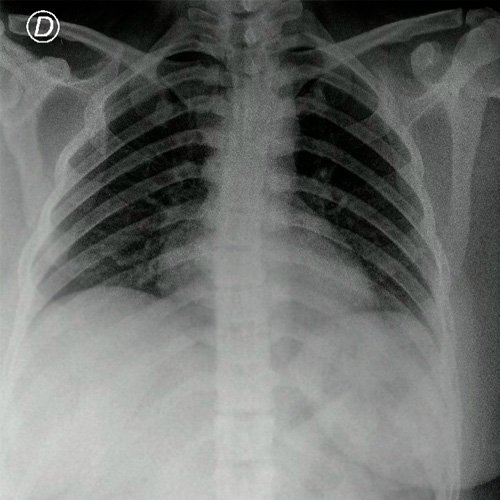
Anexo 1. Radiografía de tórax frente
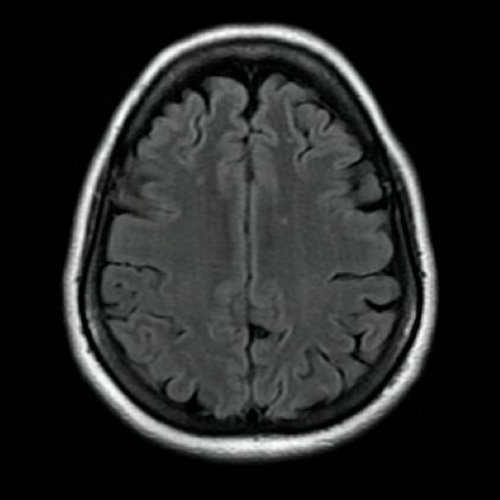
Anexo 2. Angio RMI de cráneo: Corte transversal. Secuencia t2 flair
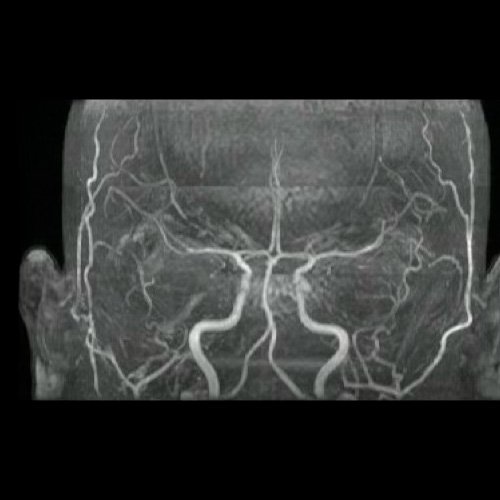
Anexo 3. Angio RMI de cráneo. Reconstrucción 3d.