Discusión del caso clínico. | Presentación |
Como objetivos de esta discusión me planteo responder a los siguientes interrogantes:
-
¿Tiene la paciente una enfermedad pulmonar intersticial difusa? Ó ¿Es una progresión de su enfermedad de base?
-
¿Cuál es el tratamiento más adecuado? ¿Es candidata a un trasplante cardiopulmonar?
-
¿Cuál es el pronóstico de su enfermedad?
Estamos frente a una paciente con antecedentes de asma, ex tabaquista de jerarquía, que en los últimos años presentó múltiples infecciones respiratorias y disnea que le impide realizar actividades de la vida cotidiana, con hallazgos tomográficos de fibrosis pulmonar y bronquiectasias.
Para introducirnos en el tema, las enfermedades pulmonares intersticiales difusas son un grupo heterogéneo de alteraciones del parénquima pulmonar, que han sido clasificadas juntas por presentar características clínicas, radiológicas, fisiopatológicas y anatomopatológicas similares. Si bien se ha empleado el término intersticial para agrupar a estas enfermedades, no es sólo el intersticio el que se ve afectado, sino toda la arquitectura pulmonar: espacios alveolares, intersticio, vía aérea de pequeño calibre y vasculatura.
En 2013 se publicó una puesta al día del consenso realizado en 2002, en el que se introdujeron las novedades en el conocimiento de la neumonía intersticial difusa y las nuevas entidades clínicas no contempladas previamente. Aunque la mayoría de entidades clínicas permanece en la nueva clasificación, se han introducido importantes cambios:
-
La neumonía intersticial no específica (NINE) idiopática se acepta como entidad clínica bien definida, con supresión del término “provisional”.
-
Las principales neumonías intersticiales idiopáticas se distinguen de las raras y de las no clasificables.
El siguiente cuadro es la clasificación del consenso del año 2013:
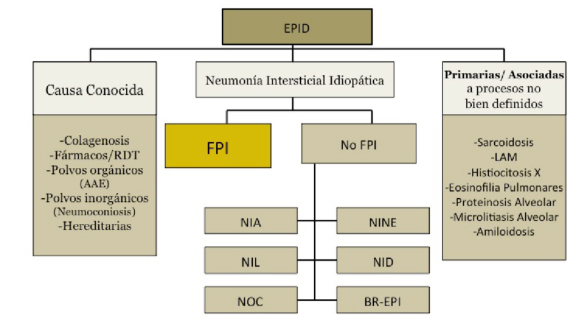
FPI: fibrosis pulmonar idiopática. NIA: neumonía intersticial aguda. NINE: neumonía intersticial no especificada. NIL: neumonía intersticial linfocítica. NID: neumonía intersticial descamativa. NOC: neumonía organizada Criptogénica. BR-EPI: bronquiolitis respiratoria asociada a enfermedad pulmonar intersticial.
Con respecto a la enfermedad pulmonar intersticial difusa de causa conocida, la paciente no presenta antecedentes de exposición a polvos orgánicos e inorgánicos así como tampoco consumo de fármacos relacionados con esta entidad, por lo que inicialmente no consideraré dichos diagnósticos. En el año 2017 se realizó en el Hospital Provincial de Centenario un trabajo donde se describió la fibrosis pulmonar como modo de presentación de enfermedades autoinmunes. En dicho trabajo se describe la importancia de realizar un interrogatorio dirigido de síntomas extra pulmonares así como de la petición del laboratorio inmunológico antes hallazgos de fibrosis en la tomografía de tórax, para poder realizar un diagnostico y así un tratamiento dirigido.


Dado a que la paciente presenta laboratorio inmunológico negativo y no presenta sintomatología extra pulmonar, haré hincapié en las neumonías intersticiales idiopáticas fibrosantes crónicas y a las relacionadas con el hábito tabáquico.
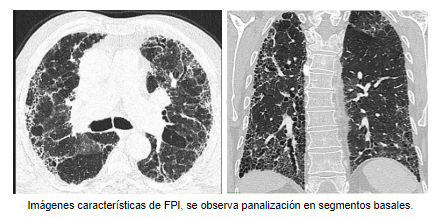
La fibrosis pulmonar idiopática es la enfermedad intersticial pulmonar más frecuente. Es de etiología desconocida, se da por agentes externos (tabaco) en personas predispuestas. Afecta principalmente al sexo masculino, con una media de 50 años de edad. Clínicamente se manifiesta de manera insidiosa con disnea progresiva, tos seca, estertores crepitantes y acropaquia. Para el diagnostico se utiliza la tomografía de tórax con alta resolución, la cual tiene un valor predictivo positivo del 95% aproximadamente cuando los hallazgos son típicos. El consenso oficial ATS/ERS/JRS/ALAT 2011 establece que, en la misma, el diagnóstico de certeza se basa en la identificación de los 4 hallazgos:
-
La afectación pulmonar debe tener un predominio basal y una localización subpleural.
-
Presencia de reticulación evidente.
-
Existencia de panalización con/sin bronquiectasias/bronquiolectasias de tracción.
-
Demostrar la ausencia de hallazgos considerados excluyentes (predominio en lóbulos superiores, peribroncovasculares, la presencia de vidrio esmerilado, micromódulos).
El rol de la fibrobroncoscopia es el de exclusión de otras entidades, y no muestra hallazgos característicos en ésta entidad.
El diagnostico se basa en los siguientes criterios (deben cumplirse los 4 criterios mayores y 3 criterios menores):
Criterios mayores:
• Exclusión de otras causas conocidas, como ciertas toxicidades de los medicamentos, exposiciones ambientales y enfermedades del tejido conjuntivo.
• Estudios de función pulmonar anormales que incluyen evidencia de restricción y alteración del intercambio gaseoso.
• Anomalías reticulares bibasales con opacidades mínimas en el vidrio esmerilado en las tomografías.
• Biopsia pulmonar transbronquial o lavado broncoalveolar que no muestra características para respaldar un diagnóstico alternativo.
Criterios menores:
• Edad > 50 años.
• Inicio insidioso de disnea de esfuerzo inexplicable.
• Duración de la enfermedad ⩾ 3 meses.
• Rales crepitantes en velcro.
Dado a que no presenta imágenes típicas de esta enfermedad en la tomografía de tórax, y a que en 4 años no ha presentado progresión de la fibrosis no lo considero un diagnóstico probable.
El fibroenfisema es un síndrome de reciente definición, caracterizado por la existencia en el mismo paciente de un patrón de enfisema en los lóbulos superiores y de fibrosis en los lóbulos inferiores. Desde el punto de vista histopatológico, la fibrosis pulmonar combinada con enfisema puede generar controversia, debiéndose establecer de forma clara la diferenciación entre los casos en que el enfisema se combina con una neumopatía intersticial fibrosante difusa, generalmente neumonía intersticial usual, de aquellos casos en los que existen áreas localizadas de fibrosis pulmonar coexistiendo con enfisema pulmonar sin asociarse en estos casos a los hallazgos clínicos o radiológicos de una enfermedad intersticial pulmonar. La incidencia es desconocida, pero se estima que representa el 5 al 10% de las enfermedades pulmonares intersticiales difusas. Se puede manifestar como bronquiolitis respiratoria asociada a enfermedad pulmonar intersticial, como neumonía intersticial descamativa o más comúnmente como neumonía intersticial usual (patrón tomográfico de fibrosis pulmonar idiopática).
La bronquiolitis respiratoria asociada a enfermedad pulmonar intersticial corresponde a la enfermedad pulmonar intersticial asociada a la lesión anatomopatológica de bronquiolitis respiratoria. En esta entidad existen manifestaciones clínicas y alteraciones tanto radiológicas como en las pruebas de función respiratoria características de la enfermedad pulmonar intersticial. Predomina en hombres, de entre 40 y 50 años, con antecedentes de tabaquismo. Clínicamente se manifiesta con disnea, estertores crepitantes en velcro y tos seca. La espirometría puede en ocasiones ser normal o evidenciar patrón restrictivo leve. En la tomografía de tórax se evidencia compromiso de los campos pulmonares superiores, con áreas de atrapamiento aéreo, nódulos centrolobulillares y vidrio esmerilado, así como engrosamiento de la pared bronquial. No se evidencia bronquiectasias, patrón de panalización ni reticulación. Su tratamiento es el cese del hábito tabáquico, con lo que la fibrosis no progresa. Los corticoides no han mostrado efectividad. Dado a que presenta clínica, hallazgos imagenológicos compatibles y detención de la fibrosis, lo considero un diagnostico probable.
La neumonía intersticial descamativa se considera para algunos autores la progresión de la bronquiolitis respiratoria asociada a enfermedad intersticial. La clínica es similar a la anterior, y mediante tomografía se manifiesta con patrón de vidrio esmerilado periférico, en bases pulmonares de manera uniforme y bien delimitada del parénquima sano. La siguiente es una tomografía típica de la neumonía intersticial descamativa.

No considero que los hallazgos tomográficos sean compatibles con ésta entidad.
La hipertensión arterial pulmonar es una complicación frecuente en el curso clínico de las enfermedades intersticiales difusas, es la principal condición que influye en su evolución y pronóstico. Se ha comunicado una prevalencia en estos pacientes que oscila entre el 47% y el 90%. En el estudio de Cottin, la presencia de hipertensión fue predictor independiente de mortalidad. La probabilidad de supervivencia a los 5 años era de 25% en los pacientes con hipertensión arterial pulmonar demostrada por ecocardiograma frente a un 75% en aquellos sin evidencia de la misma. El tratamiento con corticoides sistémicos e inmunosupresores se ha utilizado, sin haber demostrado claros beneficios en la series publicadas. La supresión completa del tabaquismo es una medida razonable que probablemente, evite la progresión de las lesiones enfisematosas.
Ahora bien, me parece importante destacar que la paciente presenta el antecedente de asma desde la infancia, con síntomas diarios de dicha afección y con infecciones respiratorias. Se calcula que el asma afecta a 300 millones de personas en todo el mundo. De ellos, alrededor del 10% padecen asma grave, y diversos estudios han demostrado que, a pesar de la disponibilidad de tratamientos eficaces, más de la mitad de los pacientes no están bien controlados en la práctica clínica habitual, lo que conlleva un aumento de la morbimortalidad y del gasto sanitario.


La paciente presenta un VEF1 < 80% y se encuentra realizando escalón 4 de la guía GINA por ello podemos concluir que la paciente presenta un asma severa y no controlada.
La causa más frecuente del control inadecuado del asma es el incumplimiento del tratamiento, en particular los corticoesteroides inhalados, posiblemente porque éstos no muestran un beneficio clínico inmediato. Se conocen además factores que dificultan el control del asma como la exposición a alérgenos, consumo de fármacos como la aspirina, inhibidores de la COX y betabloqueantes. Algunos pacientes presentan infecciones crónicas por mycoplasma pneumoniae o Chlamydia pneumoniae. Algunas mujeres presentan empeoramiento premenstrual que requiere de administración de progesterona.
En los casos de asma resistente de larga data es frecuente encontrar cambios estructurales en el árbol bronquial y parénquima pulmonar que incluye fibrosis, angiogénesis y engrosamiento de la capa muscular.
El tratamiento del asma se configura en un ciclo continuo que consta de evaluación, ajuste del tratamiento y revisión de la respuesta.
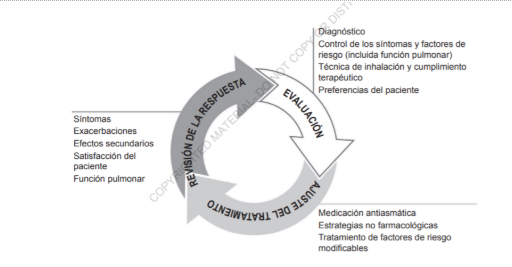
En este caso presenta buena técnica y cumplimiento terapéutico, ha controlado los factores de riesgo, como por ejemplo el cese del hábito tabáquico, pese a lo cual presenta exacerbaciones frecuentes con mala calidad de vida por lo que considero que se debe revisar el tratamiento que se encuentra realizando.
La guía GINA ha propuesto un tratamiento escalonado:

En este momento la paciente se encuentra realizando el tratamiento del escalón 4, por lo cual debería considerarse la adición de tiotropio o de montelukast, o de un tratamiento específico según el fenotipo de asma que presente.
De lo antedicho deviene la necesidad de poder caracterizar el fenotipo de los pacientes asmáticos, dado a que el mismo propone tratamientos específicos. El fenotipo final dependerá, por tanto, de las pequeñas acciones aditivas de estos genes particulares combinadas y moduladas por factores del entorno.
Los fenotipos clínicos e inflamatorios son los siguientes:
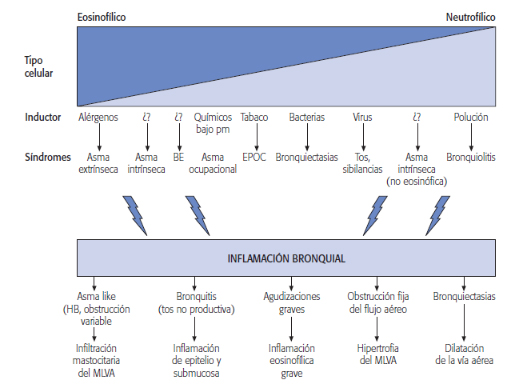
El tabaquismo activo en pacientes con asma se asocia con peor control de la enfermedad, utilización más frecuente de recursos sanitarios (mayor número de exacerbaciones, frecuentación a urgencia e ingresos hospitalarios) y descenso acelerado de la función pulmonar. Los asmáticos fumadores responden peor al tratamiento con esteroides. Las causas de esta disminución de la sensibilidad pueden ser una mayor inflamación no eosinofílica (aumento de neutrófilos en esputo), reducción de la actividad de la histona desacetilasa o deterioro en la función del receptor esteroideo. Resultados preliminares sugieren que los antagonistas de receptores de leucotrienos (sobre todo montelukast) pueden tener un efecto beneficioso mayor en pacientes fumadores con asma.
Podemos decir que la paciente presenta un fenotipo asma-EPOC (enfermedad pulmonar obstructiva crónica). La prevalencia de asma-EPOC en la población general oscila entre el 1,6 y el 4,5%, en los pacientes con EPOC entre el 12,1 y el 55,2%, y en pacientes con asma, entre el 13,3 y el 61%. No existe un criterio uniforme para su definición en pacientes con un diagnóstico previo de asma o de EPOC.
Se desconoce si la superposición de las características clínicas de EPOC y asma en un mismo paciente obedece a la coincidencia de dos enfermedades prevalentes o si, por el contrario, subyace algún elemento patogénico común. Estudios longitudinales reconocen al asma infantil como un factor de riesgo independiente para el desarrollo de EPOC, especialmente cuando coincide con el consumo de tabaco.
El grupo de pacientes con asma-EPOC englobaría tanto a los asmáticos fumadores que desarrollan obstrucción persistente al flujo aéreo, como a los EPOC con características de asma.
Esta definición engloba la necesaria coincidencia de tres aspectos básicos: la limitación al flujo aéreo persistente en el tiempo, esencial para confirmar la existencia de una obstrucción fija que no se modifica de forma espontánea o tras el tratamiento; la historia acumulada de tabaquismo (actual o pasado) como principal factor de riesgo; y las características propias del asma, entre las que se incluyen manifestaciones clínicas, biológicas o funcionales.
En cuanto al tratamiento inicial será una combinación de glucocorticoides inhalados y agonistas adrenérgicos b2 de acción prolongada (LABA). El Tiotropio (anticolinérgico) reduce el riesgo de exacerbación en la EPOC y en el asma en los pacientes insuficientemente controlados. Por otra parte, ha demostrado mejorar la función pulmonar en asmáticos en los que persiste una obstrucción bronquial a pesar de recibir tratamiento con una combinación de GCI/LABA, aunque el impacto sobre los síntomas y sobre la calidad de vida no parece clínicamente relevante. En consecuencia, se considerará la adición de tiotropio a una combinación GCI/LABA si persisten exacerbaciones y/o síntomas relevantes. No hay experiencia en asma con otros agonistas muscarínicos de acción larga (LAMA), como aclidinio, umeclidinio o glicopirronio, que son eficaces en pacientes con EPOC. Así mismo, se deberán considerar otros tratamientos complementarios, como la cesación del tabaquismo, la rehabilitación respiratoria, los antiinflamatorios nasales y la oxigenoterapia, siempre que estén indicados.
Con respecto a los hallazgos tomográficos de la paciente, resulta importante la presencia de bronquiectasias, las cuales afectan, se estima, alrededor del 30 al 40% de los pacientes asmáticos. Es posiblemente la tercera patología inflamatoria crónica en frecuencia de la vía aérea, y afecta a más de 1.100 individuos de más de 65 años por cada 100.000 habitantes. Cole plantea la existencia de un círculo vicioso tras la aparición de un evento inicial, que compromete el aclaramiento mucociliar, lo que provocaría que la mucosidad y las bacterias permaneciesen un mayor tiempo en el árbol bronquial, con la posibilidad de producir una selección de las cepas más virulentas, que lesionarían el epitelio ciliar. El proceso inflamatorio crónico resultante causaría mayor dificultad en el aclaramiento de secreciones bronquiales, facilitando las infecciones recurrentes y el daño estructural con aparición de bronquiectasia, que a su vez predisponen a nuevas infecciones, cerrando así el círculo vicioso. La consecuencia final no es otra que la progresiva obstrucción de la vía aérea y la aparición de los síntomas típicos de esta enfermedad, en especial la hipersecreción crónica y, en los estadios más avanzados, la disnea, lo cual modula la pérdida progresiva de función pulmonar y de calidad de vida de los pacientes que las padecen, llevándolos a una mortalidad precoz.
Como consecuencia de las alteraciones estructurales, las bronquiectasias generan un microambiente idóneo para el crecimiento de microorganismos cuya existencia se perpetúa por su capacidad de desarrollar mecanismos de defensa y entorpecer la acción del sistema inmune o de los antimicrobianos. La colonización bronquial se define como la presencia de una población bacteriana en la mucosa bronquial que no induce respuesta inflamatoria con repercusión clínica. Dependiendo de la identificación y permanencia en las muestras respiratorias, la colonización puede ser inicial, en el caso del primer cultivo positivo fuera de un proceso de agudización no aislado en cultivos periódicos previos; intermitente, donde aparecen cultivos alternantes positivos y negativos para un mismo germen, con al menos un mes de diferencia entre ellos; y crónica, cuando se detecta el mismo microorganismo en tres o más cultivos consecutivos y separados entre sí al menos un mes y durante un periodo de seis meses sin tratamiento antibiótico concomitante. La infección bronquial crónica supone la situación en la que una colonización bronquial genera una respuesta inflamatoria tal que provoca la aparición de síntomas claramente discernibles en el paciente que la padece. El tratamiento aconsejado cuando hay colonización inicial es la ciprofloxacina 750 mg. cada doce horas por tres semanas asociado a tobramicina o colistín vía inhalatoria por tres a cuatro meses. Para la colonización intermitente o crónica se recomienda la realización de dos a tres semanas de tratamiento antibiótico dirigido, asociado a colistín vía inhalatoria por tiempo indefinido. Además se han propuesto el uso de macrólidos ya que son efectivos en el tratamiento de la panbronquiolitis difusa y disminuyen el número de agudizaciones. Su efecto probablemente se debe a su acción moduladora de la respuesta inflamatoria y a la capacidad de interferir con la formación de biopelículas. Se recomienda su administración en la infección bronquial crónica por Pseudomonas o por otros microorganismos con control clínico difícil a pesar de un tratamiento adecuado. El fármaco con el que se dispone de mayor experiencia es la azitromicina a dosis de 250 a 500 mg. en función del peso, tres días por semana durante períodos de tres a seis meses.
Por último, es menester, dado al difícil manejo de su enfermedad de base con imposibilidad de realizar actividades de la vida, evaluar si esta paciente es candidata a recibir un trasplante cardiopulmonar. Los criterios específicos para las afecciones que presenta son los siguientes:

Dado a que no reúne los criterios y a que aún no se han intentado medidas medicas efectivas en pacientes con asma EPOC de difícil control considero que no sería candidata a recibir un trasplante cardiopulmonar.
Para concluir, considero que se trata de una paciente asma-EPOC severa de difícil control, en quien se sospechó inicialmente la presencia de enfermedad pulmonar intersticial difusa, la cual no considero probable dado a los hallazgos y a la evolución, por lo que puedo concluir diciendo presenta secuelas de su enfermedad mal controlada de larga data. Creo que se debe adecuar el tratamiento para su enfermedad de base, con el uso de tiotripio y montelukats y reevaluar la respuesta fuera de la intercurrencia infecciosa por la que está atravesando. Además, seria de suma importancia la búsqueda de colonización en el esputo, dado a que el tratamiento de las mismas disminuye drásticamente la morbi-mortalidad. Para finalizar, no considero que actualmente sea candidata a la realización de una biopsia pulmonar o trasplante cardiopulmonar.
Bibliografía:
-
Montserrat Vendrell J, Casilda O, Martínez M. A, Girón R, Máiz L, Cantón R, Coll R, Escribano A, Solé A. Diagnóstico y tratamiento de las bronquiectasias. Servicio de Neumología. Hospital Josep Trueta. Girona. España. CIBER Enfermedades Respiratorias.
-
Giugno E; Schönfeld D, Ortíz D, Baremboin E, Carles D, Martínez Cortizas, Cano L. Bronquiectasis. Comisión de Clínica y Crítica de la AAMR.
-
Tabaj G, Quadrelli S, Grodnitzky L, Sinagra. Calidad de vida en pacientes con fibrosis pulmonar idiopática. 2Hospital Británico de Buenos Aires.
-
Núñez Naveira L, Montero Martínez C, Ramos Barbón D. Oxidación, inflamación y modificaciones estructurales. Unidad de Investigación Respiratoria. Servicio de Neumología. Complejo Hospitalario Universitario Juan Canalejo. A Coruña. España.
-
Xaubet A, Molina Molina M, Ancochea J. Nueva clasificación de las neumonías intersticiales idiopáticas. Servicio de Neumologia. Hospital Clinic. Barcelona. Servicio de Neumologia. Hospital Universitario de Bellvitge. Barcelona. Servicio de Neumologia. Hospital Universitario de La Princesa. Madrid.
-
Plaza V, Álvarez F, Calle M, Casanova C, Cosío B, López-Viña , Pérez de Llano L, Quirce S, Román-Rodríguez M, Soler-Cataluña J, Miravitlles M. Consenso sobre el solapamiento de asma y EPOC (ACO) entre la Guía española de la EPOC (GesEPOC) y la Guía Española para el Manejo del Asma (GEMA). Servicio de neumología del hospital Saint.
-
Gimenez A. Síndrome de Fibrosis Pulmonar Combinado con Enfisema.
-
Recomendaciones para el diagnóstico y tratamiento de la fibrosis pulmonar idiopática. Asociación latinoamericana de tórax.
-
National Asthma Education and Prevention Program. Expert Panel Report 3: Guidelines for the Diagnosis and Management of Asthma. National institute of health.
-
Guía sobre el abordaje inicial del paciente con enfermedad difusa del Parénquima Pulmonar. Asociación argentina de medicina respiratoria.
-
Guía para el manejo y prevención del asma. Actualización 2016. Asamblea de la GINA.
-
Global initiavive for chronic obstructive lung disease. POCKET GUIDE TO COPD DIAGNOSIS, MANAGEMENT, AND PREVENTION. A Guide for Health Care Professionals 2017 EDITION.
|
Imágenes del caso
|