Discusión del caso clínico. | Presentación |
La disnea se define por la American Thoracic Society (ATS) como una experiencia subjetiva de malestar respiratorio. Su fisiopatología se asocia a condiciones en las cuales la actividad del centro respiratorio está incrementada y cuando el sistema respiratorio está sometido a carga mecánica, involucrando mecanismos centrales, periféricos y quimiorreceptores. Puede deberse al aumento de los requerimientos de oxígeno, al aumento del esfuerzo necesario para superar la resistencia pulmonar como para distender al pulmón, al deterioro neuromuscular, como a alteraciones de índole psicógeno.
La disnea se clasifica de acuerdo al tiempo de evolución en aguda, subaguda y crónica; y de acuerdo a esta clasificación sus causas son múltiples:
Agudas: embolia pulmonar, neumotórax, infarto de miocardio, edema pulmonar cardiogénico, neumonía, asma, cuerpo extraño, inhalación de tóxicos, disfunción músculo papilar, parálisis diafragmática, trastorno de ansiedad.
Crónica: (duración mayor a 4 semanas) Pulmonares: neumonías, enfermedad pulmonar obstructiva crónica, enfermedad pulmonar restrictiva, enfermedad intersticial, derrame pleural. Cardíacas: disfunción ventricular, derrame y taponamiento cardiaco. Otras: anemia, intoxicación con salicilatos, etilenglicol, desórdenes neuromusuclares.
Subagudas: patologías crónicas descompensadas.
Es importante analizar las cirscunstancias de aparición, la posición en la cual se exacerba, como otros factores precipitantes, su duración, progresión, variaciones diurnas y estacionales, que factores la alivian o la predisponen (como el tabaquismo, las exposiciones laborales, comorbilidades y los antecedentes familiares).
Para su diagnóstico es importante tener presente que solo con la historia clínica y el primer nivel de estudios se puede orientar el diagnóstico hasta en el 80% de los pacientes. Para ello contamos con radiografía de tórax, la cual es útil orientando a enfermedad parenquimatosa pulmonar, patología pleural y de caja torácica. Para el diagnóstico de síndromes restrictivos, el patrón oro es el estudio de volúmenes pulmonares y el diagnóstico se justifica con una capacidad pulmonar total disminuida. Si ésta se asocia con aumento del volumen residual y de su relación con la capacidad pulmonar total, la orientación es hacia una enfermedad neuromuscular.
La espirometría examen funcional respiratorio (EFR) otra herramienta útil para el diagnóstico de enfermedad obstructiva (EPOC). Puede ser reversible (respuesta a broncodilatadores positiva) o no reversible y progresiva, lo cual apunta al diagnóstico de EPOC. Una enfermedad obstructiva con una difusión de monóxido disminuida aproxima el diagnóstico final hacia enfisema pulmonar, cuya confirmación se realiza con una tomografía computarizada de alta resolución.
Con respecto al diagnóstico de enfermedad vascular pulmonar, el ecocardiograma con Doppler es de utilidad, ya que permite estimar la presión en la arteria pulmonar ante la presencia de regurgitación tricuspídea. El ecocardiograma bidimensional, el electrocardiograma y el BNP (péptido natriurético cerebral o péptido natriurético tipo B) son útiles en el diagnóstico de insuficiencia cardiaca como casa de disnea. En algunos pacientes con enfermedad coronaria, la disnea puede representar un equivalente anginoso y debe evaluarse con los métodos diagnósticos menos invasivos hasta el cateterismo cardíaco.
Si se sospecha tromboembolia pulmonar (TEP), el centellograma V/Q, el eco Doppler de miembros inferiores, la angio-TAC o la arteriografía permiten aproximar y/o certificar el diagnóstico.
Respecto a la presencia de un dímero D elevado tiene un valor predictivo positivo del 29% para la existencia de enfermedad tromboembólica y un valor predictivo negativo del 98% para la ausencia de enfermedad tromboembólica. Es utilizado ante la baja probabilidad, siendo excluido si es negativo y requiriendo métodos complementarios (Angio-tomografía) de ser positivo.
Luego de este breve repaso podemos inferir que nuestro paciente que presentó una disnea aguda, en el contexto de reposo absoluto por un cuadro de lumbalgia, junto a la presencia de un valor de dímero D elevado, el primer diagnóstico diferencial es el tromboembolismo pulmonar.
La enfermedad tromboembólica venosa (TEV) involucra la trombosis venosa profunda (TVP) y el tromboembolismo pulmonar (TEP).
El análisis siempre debe empezar por la probabilidad clínica del diagnóstico TVP/TEP, basándose en los factores de riesgo presentes: antecedentes de TEV anteriores, edad avanzada (>70 años), cáncer activo (especialmente pulmón, páncreas, colorrectal, riñón y próstata), poca movilidad por trauma o cirugía reciente, daño neurológico o uso de férulas de inmovilización, viajes prolongados, portadores de catéteres intravenosos, embarazo, anticonceptivos orales o terapia de reemplazo hormonal con estrógenos, obesidad, trombofilias adquiridas (mutación de factor V Leiden o gen de protrombina y deficiencias de proteina S, C o antitrombina), síndrome antifosfolípidos, insuficiencia cardíaca congestiva, enfermedad inflamatoria intestinal, síndrome nefrótico, hiperhomocisteinemia, policitemia vera, trombocitosis esencial o hemoglobinuria paroxística nocturna.
La trombosis venosa profunda se presenta como dolor y edema localizado a lo largo del sistema venoso profundo de extremidades inferiores o superiores. Las principales complicaciones de la TVP son el TEP y el síndrome post-trombótico. La tromboflebitis superficial también debe incluirse en este espectro patológico, ya que hasta en 25% de los casos hay TVP concomitante. Un examen de dímero-D con sensibilidad apropiada (ELISA o método turbidimétrico avanzado) en un paciente con baja probabilidad clínica, descarta TVP con tranquilidad. Los pacientes con probabilidad clínica moderada o alta deben someterse a una ecografía doppler color venosa de toda la extremidad para excluir o confirmar el diagnóstico. En localizaciones centrales como región subclavia o pelviana se pueden requerir imágenes adicionales como tomografía computada o resonancia magnética.
De todas las TVP proximales de extremidades inferiores, 50% embolizan al pulmón, muchas veces en forma asintomática. Los síntomas que más frecuentemente se asocian con TEP son disnea, dolor torácico tipo pleurítico, hemoptisis, síncope y tos. Al examen físico los pacientes pueden presentar taquipnea, taquicardia e hipotensión. En la radiografía de tórax (habitualmente normal) puede verse hemidiafragma elevado por pérdida de volumen pulmonar, opacidades segmentarias, derrame pleural o atelectasias lineales. El electrocardiograma (alterado en menos de 10% de las veces) puede mostrar taquicardia sinusal, S1Q3T3, desviación del QRS a derecha, BCRD transitorio, inversión de ondas T y depresión del segmento ST en percordiales derechas. En los gases arteriales, que pueden ser normales hasta en 40% de los TEP, puede existir hipoxemia, hipocapnia y aumento de la diferencia alvéolo-arterial de oxígeno.
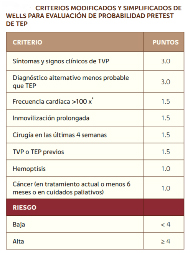
Al enfrentar un paciente con sospecha de TEP se deben analizar los factores de riesgo y los elementos clínicos para llegar a una apuesta de probabilidad clínica. Se recomienda siempre implementar en Servicios de Urgencia algún sistema de puntuación de probabilidad diagnóstica de TEP previo a los exámenes (dímero-D o angioTAC). El más utilizado es el Puntaje de Wells Simplificado, separa a los pacientes en dos grupos de riesgo: bajo y alto. Al igual que en TVP, si la probabilidad clínica es baja para TEP y el dímero-D es normal, no se requiere más estudio ni tratamiento, ya que el valor predictivo negativo (VPN) es 99%.
Existe evidencia actual que sugiere que el punto de corte del dímero-D debe ajustarse por edad en pacientes sobre 50 años. Si el punto de corte es 500 mcg/L, se debe multiplicar por la edad por 10 (es decir a los 60 años el valor normal es 600 mcg/L y a los 75, 750 mcg/L). Si la probabilidad clínica es alta o el dímero-D está elevado, se debe realizar una angiotomografía computada (angioTAC) de tórax helicoidal multicorte, con protocolo de TEP, que tiene sensibilidad y especificidad mayores a 95%, con un VPN a tres meses de 99%. En pacientes con contraindicación absoluta de medio de contraste por anafilaxia o insuficiencia renal, se puede usar un centellograma V/Q si no hay opacidades parenquimatosas ni derrame pleural que interfieran con la interpretación (examen de primera línea en embarazo por menor radiación). Una ecografía doppler positiva para TVP en paciente con alta probabilidad clínica de TEP certifica diagnóstico sin necesidad de más imágenes (conducta útil en embarazo, período en que el dímero-D pierde rendimiento y mayor riesgo por radiación del angioTAC).
Entonces bien, ¿Estamos ante un paciente con enfermedad tromboembolica? En el caso en particular si bien presentaba a favor factores de riesgo como inmovilización en el contexto de lumbalgia, insuficiencia cardiaca; un cuadro clínico compatible de TEP con disnea aguda, edemas de miembros inferiores (si bien era simétrico), un valor elevado de Dímero D, junto a gasometría compatible (hipoxemia e hipocapnia; debemos tener en cuenta que en contra de dicho diagnóstico presentaba la ausencia de edemas asimétricos en miembros inferiores, como ausencia de patrón S1Q3T3 a nivel del electrocardiograma y ausencia de alteraciones morfológicas en las cavidades derechas a nivel del ecocardiograma. Por lo tanto ante un puntaje de Wells ampliado alto, se requirio continuar con algoritmo diagnóstico realizando angiotomografía multicorte con protocolo de TEP, la cual descartó el diagnóstico.
Es importante destacar la existencia de otras causas de elevación de Dímero D: tromboembolia venosa, coagulopatias de consumo, sepsis, embarazo, infarto de miocardio, insuficiencia cardiaca congestiva, neoplasias, leucemias aguda, colagenopatías, postoperatorio, hepatopatía, traumatismos, reposo prolongado y la edad avanzada, por lo tanto nuestro paciente presenta causas alternativas de elevación de Dímero D diferentes a la enfermedad trombembólica.
Dentro de las otras causas de disnea aguda y subguda a descartar se encuentran:
- Infarto agudo de miocardio, Teniendo en cuenta la disnea como equivalente del dolor anginoso, nuestro paciente presentaba laboratorio enzimático, electrocardiograma y ecocardiograma sin evidencia de isquemia aguda, siendo poco probable tal diagnóstico.
- Insuficiencia cardiaca congestiva: presentando a favor de dicho diagnóstico la presencia de disnea clase funcional II de tipo crónica que aumento el último mes, estertores crepitantes bilaterales basales al ingreso, edemas en miembros inferiores de carácter intermitente y simétrico, como así también la presencia de cardiomegalia a nivel de la radiografía de tórax. Sin embargo presentó valores normales de péptido natriuretico B (PNB), ecocardiograma con fracción de eyección conservada y mejoría clínica sin requerimiento diurético. Descartando por lo tanto el cuadro de Edema pulmonar cardiogénico.
- Neumonías: diferenciando aquellas típicas, habitualmente causada por Streptococcus pneumoniae, caracterizada por un cuadro muy agudo con fiebre acompañada de escalofríos y síntomas respiratorio predominantes (tos-expectoración purulenta), junto a opacidades pulmonares a nivel radiográfico; de aquellas atípicas, de presentación subaguda, con fiebre sin escalofríos, o febrícula, síntomas respiratorios no muy importantes, entre los que se destaca la tos irritativa, coexistiendo con manifestaciones extrarrespiratorias en ocasiones bastante abigarradas, en ocasiones con opacidades pulmonares intersticiales a nivel radiográfico, cuya etiología más frecuente está dada por Mycoplasma pneumoniae, Chiamydia psittacci, Chiamydia pneumoniae y Coxiella burnetii.Sospecho que si bien nuestro paciente no presentó síntomas respiratorios, sensación febril, como así tampoco leucocitosis o aumento significativo de reactantes de fase aguda, ni realizó tratamiento antibiótico para su mejoría; las neumonías atípicas son un diagnóstico probable y se deberá aguardar los resultados serológicos para arribar a su exclusión definitiva.
Con respecto a su disnea crónica basal resulta interesante considerar su etiología, diferenciando causas pulmonares (enfermedad pulmonar obstructiva, enfermedad pulmonar restrictiva, enfermedad pulmonar intersticial, derrame pleural), cardíacas: (disfunción ventricular, derrame y taponamiento cardiaco), y otras causas como anemia, intoxicación con salicilatos, etilenglicol y desórdenes neuromusculares. Pondré énfasis en primera instancia a las causas pulmonares basándome en los hallazgos tomográficos de vidrio esmerilado, diferenciando en primera instancia los tipos de patrones pulmonares.
Patrones pulmonares difusos: (clasificación de Felson/Fleischener): se dividen en 4 grupos.
- Patrón de la vía respiratoria: donde existe obstrucción completa o parcial de la vía respiratoria, dentro de este se encuentran las atelectasia, el atrapamiento o la pequeña vía aérea.
- Patrón vascular: presenta ausencia de opacidades lineales o nodulares. Existe un afinamiento de vasos y ramificación a medida que divergen; incluyen al cortocircuito izquierda-derecha, la hipertensión arteria pulmonar e hipertensión venocapilar.
- Patrón intersticial: presencia de engrosamiento del tejido intersticial con acúmulo o infiltración por líquido, células inflamatorias, células neoplásicas o material proteináceo. El patrón intersticial a su vez puede según a su forma de distribución ser orientativo de su etiología, por ello:
-Lineal y reticular: causado tanto por inflamación (colagenopatías, infecciones, idiopático), fibrosis (post-inflamatoria, post-radiación), y por edema.
-Patrón nodular:
PERILINFATICA: visualizado en casos de linfangitis carcinomatosa, sarcoidosis, silicosis, neumonitis intersticial linfoidea y amiloidosis.
ALEATORIA: tuberculosis miliar, metástasis hematógena y micosis.
CENTROLOBULILLAR: neumonía por hipersensibilidad, bronquiolitis por tabaquismo, infecciones de diseminación endobronquial, carcinoma bronquioloalveolar.
-Patrón con disminución de la densidad: (la más frecuente es la fibrosis pulmonar), bronquiectasias, enfisema, quistes pulmonares, patrón en panal.
Y por último:
Patrón alveolar: con aumento de la opacidad pulmonar. dividido en consolidación, mosaico, vidrio esmerilado y el tipo crazy paving. Además pueden ser:
-Localizados: encontrados en la neumonía, contusión pulmonar, infarto pulmonar o cáncer bronquioalveolar.
-Difusas: en edema agudo de pulmón, neumonías atípicas.
Dentro de ellos en consideración a los hallazgos tomográficos en nuestro paciente de vidrio esmerilado, orientativo tanto de patrón intersticial como de patrón alveolar, ambos por su distribución difusa nos obliga a descartar causas inflamatorias (sean infecciosas, como las ya mencionadas neumonías atípicas; como colagenopatías) causas poco probables ante un laboratorio sin leucocitosis, con reactantes de fase aguda normales, y perfil inmunológico dentro de parámetros normales (factor reumatoide, anticuerpos citrulinados, ANCA, FAN); como así también descartar edema pulmonar, con clínica e imagen compatible a la de nuestro paciente de carácter aguda, dentro de ellas, si bien presenta antecedentes de cardiopatía isquémica ya se descartó como me explayé iniciáleme la causa cardíaca; restando considerar las causas de edema pulmonar no cardiogénico, que especificaré más adelante. Otras causas a descartar son las causas metastásicas, no encontrándose imágenes pulmonares nodulares compatibles.
En el caso de nuestro paciente para mayor aproximación diagnóstica se realizó además una espirometría que resultó con patrón restrictivo. Recordar que dicho patrón se refiere a la restricción de la expansión pulmonar tanto por alteraciones del parénquima como extra-parenquimatosas, y dentro de sus causas puede deberse tanto a mala técnica, a enfermedades pulmonares intersticiales, a resecciones pulmonares, como a patologías no pulmonares (alteración de la caja torácica, obesidad, alteraciones neuromusculares, patologías pleurales y diafragmáticas y a insuficiencia cardiaca). Dicho esto la espirometría del paciente nos orienta a patología del parénquima pulmonar y dentro de ellas me centraré en primera instancia en las enfermedades intersticiales.
Haré mención a alguna de ellas:
Enfermedad pulmonar intersticial: (EPI) o enfermedades pulmonares parenquimatosas difusas, resultan del daño de las células que rodean los alvéolos pulmonares, causando inflamación y fibrosis en los pulmones. Existen más de 300 enfermedades clasificadas como enfermedades pulmonares intersticiales. La mayoría son muy raras. Se reconoce que los factores ambientales son la causa de aproximadamente el 35 %.
Las formas más comunes de EPI son la fibrosis pulmonar idiopática y la sarcoidosis, ya que suponen el 50% de todas las EPI, continúan la alveolitis alérgica extrínseca y la asociada a enfermedad del colágeno.
Puede diferenciarse tanto una forma crónica con clínica gradual, disnea de esfuerzo progresiva, tos seca, alteraciones en la radiografía de tórax, estertores crepitantes, acropaquía (30%), y manifestaciones extra pulmonares; como una forma aguda o subaguda, presentándose con fiebre y síntomas sistémicos. Dentro de ellas, las más destacables respecto al caso de nuestro paciente se encuentran la neumonía intersticial aguda (NIA), neumonía intersticial no específica, alveolitis alérgicas extrínsecas, neumonitis por fármacos, neumonía organizada criptogenética (NOC); y las eosinofilias pulmonares.
Fibrosis pulmonar idiopática: definida como la presencia de neumonía intersticial usual (NIU) en la histología pulmonar. Esta es la más frecuente, con una prevalencia: 20/100.000 hab/varones, dentro de su clínica se presenta con disnea progresiva, tos seca, estertores crepitantes, acropaquia, una radiografía de tórax con opacidades reticulares, que predominan en bases pulmonares, bilaterales. Para su diagnóstico se requiere tomografía de alta resolución (TACAR), la cual presenta una sensibilidad 90%, y un lavado broncoalveolar con la presencia de neutrofilia asociada o no a eosinofilia. Es una patología de mal pronóstico: 50% fallecen a los 3-5 años. Como único tratamiento médico posible al momento se encuentra la pirfenidona, con resultados controversiales, ya que no modifica el pronóstico; y como alternativa se encuentran los corticoides junto a la azatioprina. ¿Acaso nuestro paciente podría presentar esta patología? Considero que solo presenta a favor la edad de la presentación que generalmente es en mayores de 50 años, el probable patrón intersticial en tomografía y una espirometría de tipo restrictiva. Pero debemos tener en cuenta que generalmente es una patología progresiva, no de forma aguda como presento nuestro paciente, suele predominar en bases pulmonares, nuestro paciente presenta alteración difusa homogénea del parénquima, además de una mejoría sin mediar tratamiento; lo que definitivamente aleja el diagnóstico.
Neumonía intersticial no específica (NINE): su clínica suele ser insidiosa-subaguda, con presencia de acropaquía, su etiología es idiopática o asociada drogas, colagenopatías, y en las imágenes puede hallarse vidrio deslustrado simétrico y basal, el lavado bronco-alveolar no arriba al diagnóstico y se requiere biopsia. Presenta mejor pronóstico a pesar de su gravedad. Este diagnóstico lo considero poco probable.
Neumonía intersticial aguda (NIA) (Harmmanrich): Se presenta como un distrés agudo idiopático con daño alveolar difuso, su etiología suele ser variada (infecciosa, inhalación de tóxicos, fármacos, radioterapia y colagenopatías), y su clínica inicia con un síndrome gripal que evoluciona a distrés con rapidez requiriendo ventilación mecánica. Para llegar al diagnóstico las imágenes nos muestran infiltrados alveolares bilaterales. (TACAR con vidrio deslustrado y consolidación.). Presenta un mal pronóstico (50% muerte a los 2 meses) Claramente en su inicio el paciente no presento síndrome gripal, ni evoluciono hacia el requerimiento ventilatorio, considero poco probable dicho diagnóstico.
Respecto al laboratorio nos permitió ante la ausencia de eosinofilia (descartar eosinofilias pulmonares), la ausencia de aumento de LDH (hacia proteinosis alveolar y otras EPID), la ausencia de hipercalciuria y la hipercalcemia (descarta Sarcoidosis), enzimas musculares en valores normales y el Ac anti Jo 1 negativo (descarta Dermatomiositis y polimiositis), un factor reumatoide negativo (Artritis reumatoide), Ac antitisulares negativos (Lupus eritematoso sistémico), Ac anti ENA- Ac SC 70, Ac antiendomisio negativos descartan esclerodermia.
Otras entidades como neumoconiosis, debidas a la inhalación de agentes en el lugar de trabajo (polvo de sílice “silicosis”, el polvo de carbón “neumoconiosis del minero de carbón”; y el amianto “asbestosis”, provocando una cicatrización generalizada y el endurecimiento (fibrosis) de los pulmones. Enfermedades en la actualidad menos comunes debido a los cambios en las prácticas industriales. Si bien el paciente es albañil y se desarrolló como pintor exponiéndose a aerosoles por un largo período, no estuvo expuestos a estas sustancias inorgánicas en particular.
La alveolitis alérgica extrínseca se debe a una reacción alérgica a la inhalación de varios agentes orgánicos; las causas más comunes incluyen la exposición al polvo de heno enmohecido (pulmón de granjero) o de palomas o pájaros en cautiverio (pulmón del cuidador de aves). Nuestro paciente no se encontró expuesto a ellos como así tampoco a animales de cría, dentro de su hogar o cercano al mismo.
Y por último ciertos medicamentos pueden causar enfermedades pulmonares intersticiales. Entre los más comunes se encuentran: amiodarona, bleomicina, metotrexato y la nitrofurantoína. El paciente no se encontraba bajo tratamiento con dichos fármacos.
Retomando al edema pulmonar no cardiogénico como otra entidad que deseo considerar en nuestro paciente, esta se presenta generalmente en adultos mayores de 60 años, sin antecedentes de cardiopatía, ni clínica compatible con insuficiencia cardíaca congestiva descompensada, con presencia de venas cervicales aplanadas, un electrocardiograma con taquicardia sinusal, o cambios inespecíficos del segmento st, una radiografía de tórax con infiltrados periféricos, y con pedículo vascular menor a 48 mm, broncograma aéreo, y una presión arteria pulmonar normal, índice cardíaco conservado; además en el laboratorio presenta valores de Peptido natriurético tipo B bajos (< 100 pg/ml). Dentro de su fisiopatología la presión hidrostática es normal, por lo cual el líquido se desplaza con la proteína conforme cambia la fuerza oncótica del vaso hacia el tejido. Como causas se encuentran: edema pulmonar de la altura, pulmón neurogénico, pulmón nefrogénico, síndrome de distres respiratorio del adulto, infecciones (neumonía, hantavirus), tóxicos o drogas, radiación, neumonitis post radiación, síndrome del ahogamiento, por re-expansión pulmonar, neumoconiosis, linfangitis carcinomatosa, otros: eclampsia, postcardioversión, postbypass. Considero que nuestro paciente el cual se encontraba bajo tratamiento con opiodes (metadona), por la lumbalgia, puede haber desencadenado un cuadro de edema pulmonar no cardiogénico, que presentó mejoría tras la suspensión del mismo.
La metadona es uno opioide sintético introducido en 1940, agonista mu, con una vida media prolongada, por lo cual se utiliza para el manejo del dolor crónico, presenta un inicio de acción: 10-20 minutos, con un metabolismo hepático y una excreción por bilis y orina, su vida media es de 15 a 40 hs, y sus efectos adversos son similares para el resto de los opioides. Por consiguiente considero probable que este fármaco haya descompensado un pulmón con patología basal.
Por otro último nuestro paciente presenta un cuadro de lumbalgia, sin diagnóstico al momento, por lo que haré una breve reseña sobre el tema y etiologías a considerar:
Lumbalgia: se define como un síndrome musculoesquelético, cuyo principal síntoma es la presencia de dolor focalizado en el segmento final de la columna vertebral (zona lumbar). En la mayoría de los pacientes suele ser inespecífico, y tales pacientes mejoraran en pocas semanas con un tratamiento conservador sin precisar pruebas complementarias. La lumbalgia es la causa más frecuente de incapacidad en la población comprendida entre los 16 y 44 años. Puede afectar al 84% de las personas en algún momento de su vida. Menos del 1% de los pacientes con lumbalgia tendrá una etiología sistémica grave (neoplasias u osteomielitis); y menos del 10% corresponden a etiologías menos graves como fracturas por compresión vertebral, radiculopatía o estenosis espinal.
Hay varias clasificaciones:
-dependiendo de si se llega a conocer o no la causa de la lumbalgia (específica e inespecífica),
-de las características del dolor (mecánico e inflamatorio) y
-de la duración del dolor (agudo si dura menos de 4 semanas, subagudo, con una duración entre 4 y 12 semanas y crónico, cuando la duración es superior a 12 semanas).
-de la irradiación (lumbalgia simple: cuando el dolor no se irradia hacia los miembros inferiores y es de localización fija, y lumbalgia irradiada: cuando el dolor ser irradia hacia la pierna, por debajo de la rodilla, lo que conocemos como ciática).
Es en ésta clasificación donde radica la importancia de la anamnesis y el examen físico inicial, ya que los casos de lumbalgia no mecánica, si bien representan menos del 3%, revisten vital importancia debido a que pueden ser el primer o principal síntoma de patologías graves.
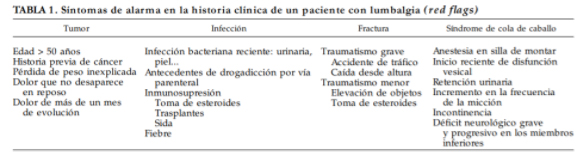
La mayoría de las guías recomiendan el uso de signos de alarma o banderas rojas, que ayuden a identificar a aquellos pacientes con mayor posibilidad de patologías graves, y que luego pasan a ser candidatos para exámenes diagnósticos más intensivos.

Tener presente que en cualquier paciente con síntomas radiculares o compresión de la cola de caballo o déficit neurológico grave debe solicitarse una resonancia magnética inmediata. Otros pacientes que requieren un estudio radiológico o analítico inmediato son los que tienen un alto índice de sospecha de infección espinal, una historia actual o reciente de neoplasias, factores de riesgo para las mismas, y aquellos con sospecha de fractura vertebral, o en el caso de lumbalgia crónica (pacientes que no han mejorado después de cuatro a seis semanas de tratamiento conservador inicial se vuelven a evaluar y, dependiendo de los síntomas presentes, se deciden las pruebas complementarias oportunas, al igual que los pacientes con un dolor lumbar crónico de más de 12 semanas de evolución).
Por tanto, no está indicado realizar pruebas complementarias de forma sistemática durante el primer mes de evolución, salvo que exista la sospecha de la existencia de procesos específicos no banales, entre ellos la fiebre, el cuadro constitucional, un síndrome miccional o alteraciones en el flujo urinario, la persistencia o el empeoramiento del dolor en reposo o por la noche, o la presencia de alteraciones objetivas neurológicas acompañantes.

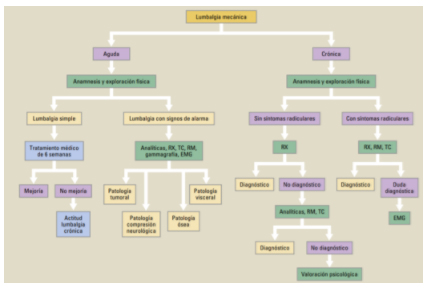
Dentro de los estudios complementarios a solicitar: la radiografía simple de columna lumbar en proyección anteroposterior y lateral es poco específica. Puede ayudar a determinar la presencia de fracturas, cambios degenerativos, curvas o deformidades. Las radiografías no brindan información en los trastornos musculares, ligamentosos, discos y nervios. Por su parte, la resonancia magnética muestra, detalladamente, los componentes de la columna. Es de gran utilidad para evaluar problemas en los discos lumbares y las raíces nerviosas, y también para descartar otras causas de la lumbalgia tales como infecciones espinales o tumores. La tomografía computadorizada permite una mejor valoración del hueso. Posibilita visualizar hernias discales, estenosis vertebrales secundarias a artrosis y fracturas vertebrales. Por último, la gammagrafía ósea se realiza a través de la administración intravenosa de fosfonatos marcados con Tecnecio 99, puede ser utilizada cuando las radiografías de columna son normales pero la clínica orienta a osteomielitis, neoplasia o fractura oculta.
En la lumbalgia mecánica, las pruebas analíticas solo son necesarias en casos excepcionales. Se suele solicitar velocidad de sedimentación globular, proteína C reactiva, prueba de Mantoux, HLA-B27 y proteinograma por electroforesis, en casos de lumbalgia inflamatoria. Si la sospecha es de una espondilodiscitis, se realizará una prueba de Mantoux, hemocultivos y serología para Brucella. Otras determinaciones analíticas y exploraciones complementarias que se pueden solicitar son el estudio del balance calcio-fósforo, vitamina D3, niveles de PTH, fosfatasa alcalina en caso de sospecha de enfermedad de Paget ósea o estudio de osteoporosis ante evidencia de fracturas. En los pacientes con dolor lumbar que tienen factores de riesgo para neoplasias, evaluamos la velocidad de sedimentación globular o proteína C reactiva y se solicitan pruebas de imagen oportunas (radiografía, resonancia magnética, gammagrafía ósea).
En el estudio de Van Den Hoogen et al sobre los síntomas y signos de tumoraciones espinales se comprueba cómo las preguntas que se deben realizar al paciente ante una lumbalgia (red flags-banderas rojas para tumor; tabla 1) presentan una especificidad del 70% y una sensibilidad del 50%.
En ausencia de datos positivos que apunten hacia un problema grave, la mayoría de las lumbalgias suele ser benigna, y como indica la Guía Americana de Bigos de 1994, ante una lumbalgia aguda, sin criterios de banderas rojas, se debe recomendar al paciente, como máximo, 4 días de reposo en cama, pues más tiempo conlleva que el paciente crea que es portador de una enfermedad importante.
Hay que recordar que entre el 5 y el 10% de las lumbalgias se cronifican (duración mayor de 12 semanas), lo que genera aumento del coste personal, sanitario y social. El mayor riesgo personal, laboral y psicosocial no está en la cronificación del dolor, sino en la cronificación de la incapacidad.
Por lo tanto en el caso de nuestro paciente con un cuadro de lumbalgia mayor a 4 semanas, considerada crónica, sin síntomas radiculares solicitaría inicialmente una radiografía simple de columna y si la misma no clarifica el diagnóstico proseguiría a una resonancia magnética intentado dilucidar su etiología debido a la presencia de banderas rojas como la edad de presentación, la existencia de factores de riesgo (tabaquismo), su duración mayor a 4 semanas, y la persistencia a pesar del reposo y requerimiento de drogas opiodes para su tratamiento, con respuesta parcial a los mismos; siendo imprescindible tal estudio.
Por consiguiente propongo
-
Suspender el tratamiento con opiodes (metadona).
-
Abandono de inmediato el hábito tabáquico.
-
Aguardar resultados de serologías virales.
-
Considerar tomografía de control en tiempo prudencial.
-
Continuar estudios de la lumbociatalgia (radiografía, resonancia magnética).
-
Prevención laboral.
Bibliografía:
-Disnea, Richard M. Schwartzstein, Harison 19° edicion, capítulo 47,
Prosac,Módulo 7 – Fascículo Nº 1 – 2011 83 Disnea: aspectos fisiopatológicos y aproximación diagnóstica Dra. Patricia Aruj, Dr. Edgardo Sobrino y Dr. Guillermo Semeniuk European lung foundation, White book, ILDs, diciembre 2013
- [REV. MED. CLIN. CONDES - 2015; 26(3) 338-343] DIAGNÓSTICO Y TRATAMIENTO DEL TROMBOEMBOLISMO PULMONAR DIAGNOSTIC AND MANAGEMENT OF ACUTE PULMONARY THROMBOEMBOLISM DR. JORGE SANDOVAL B. (1), DR. MATÍAS FLORENZANO V. (1) (2) (1) Instituto Nacional del Tórax (2) Centro de Enfermedades Respiratorias Adulto. Departamento de Medicina Interna. Clínica Las Condes 2015, 26 (3) (338-343).
- REVISIÓN Neumonías atípicas R. Irigaray y J. Dorca Servicio de Neumología. Ciudad Sanitaria Universitaria de Bellvitge. Universidad de Barcelona.
-VARELA, Brenda et al. Manejo de las enfermedades intersticiales en Argentina: Una encuesta a neumonólogos. Rev. am. med. respir. [online]. 2015, vol.15, n.3 [citado 2017-08-03], pp. 171-189 . Disponible en: <http://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S1852-236X2015000300004&lng=es&nrm=iso>. ISSN 1852-236X.
-American college of physicians and the american pain society. Clinical Guidelines: Nonpharmacologic Therapies for Acute and Chronic Low Back Pain: A Review of the Evidence. Ann Intern Med 2007; 147: 492-504.
-Andersson GBJ. Epidemiologic features of chronic low-back pain. Lancet 1999; 354: 581-5.
-Nuevos conceptos sobre las lumbalgias y guías de práctica clínica J.L. Peña Sagredoa y A. Humbría Mendiolab aServicio de Reuma tología . Hospita l Universita rio Ma rqués de Va ldecilla . Depa rta mento de Medicina y Psiquia tría . Universida d de Ca nta bria . Sa nta nder. bServicio de Reuma tología . Hospita l Universita rio de la Princesa . Universida d Autónoma de Ma drid. Espa ña .
-Protocolo diagnóstico del dolor lumbar mecánico A. Movasat Hajkhan*, C. Bohórquez Heras, A. Turrión Nieves y M. Álvarez de Mon Soto Enfermedades del Sistema Inmune-Reumatología. Hospital Universitario Príncipe de Asturias. Alcalá de Henares. Madrid. España. Departamento de Medicina y Especialidades Médicas. Universidad de Alcalá de Henares. Alcalá de Henares. Madrid. España.
- García-Morales MA, Tena D, Gil AM, Fernández-Bravo C, Velasco AM. Dolor lumbar DTM grupo científico. En: Rodríguez JL, editor. Medicina Interna. Vol 2. Madrid: Marban; 2015. p. 1152-62.
|
Imágenes del caso
|